바이오산업동향
- 등록일
- 2020-09-18
- 작성자
- 의생명공학과
- 조회수
- 1187

‘Closed’ and ‘open’ conformations of the spike protein on SARS-CoV-2, which binds to receptors on human cells. A common mutation (D614G; left) seems to make the protein favour open conformations, which might mean the virus can enter cells more easily. Source: Structural data from K. Shen & J. Luban / ⓒ Nature
많은 연구자들의 생각은 '만약 어떤 변이가 바이러스의 더욱 신속한 확산에 도움이 됐다면, 그것은 초창기에(인간에게 최초로 점프할 때, 또는 사람들 사이에서 효율적으로 이동하는 능력을 획득했을 때) 일어났을 것'이라는 것이다. 모든 지구촌 사람들이 바이러스에 취약했던 시절, '바이러스가 더 잘 확산되어야 한다'는 진화압력은 거의 존재하지 않았을 것이다. 그러므로 심지어 '잠재적으로 유익한 변이'일지라도 번성하지 않았을 것이다. "바이러스의 입장에서 볼 때, 마주치는 사람들마다 예외 없이 좋은 먹잇감이었을 것이다"라고 하버드 공중보건대학원의 윌리엄 해니지(역학)는 말했다. "초창기의 상황을 이보다 더 잘 설명할 수 있는 선택이론은 없다." (1편에서 https://ibric.org/myboard/read.php?Board=news&id=321469&SOURCE=6)
'G 바이러스'는 'D 바이러스'보다 더 빠르게 확산될까?
D614G가 빠르게 확산되는 것을 목격했을 때, 코버는 '유의미한 자연선택의 사례를 발견했구나'라고 생각했다. 그 변이가 그녀의 눈길을 끈 이유는, 스파이크 단백질에 위치하기 때문이었다. 스파이크 단백질로 말하자면, (바이러스에 결합하여 감염성을 제거하는) 중화항체의 주요 표적이다. 게다가 D614G를 보유한 바이러스의 출현빈도는 지구상의 몇몇 지역에서 증가하고 있었다.
D614G는 지난 1월 말 중국과 독일에서 수집된 바이러스에서 처음 포착되었고, 대부분의 과학자들은 그 변이의 원조가 중국이라고 생각했다. 그것은 현재 3개의 다른 변이들(SARS-CoV-2 유전체의 다른 부분에 존재함)을 동반하는데, 이는 대부분의 D614G 바이러스들이 공통조상을 보유하고 있음을 시사한다.
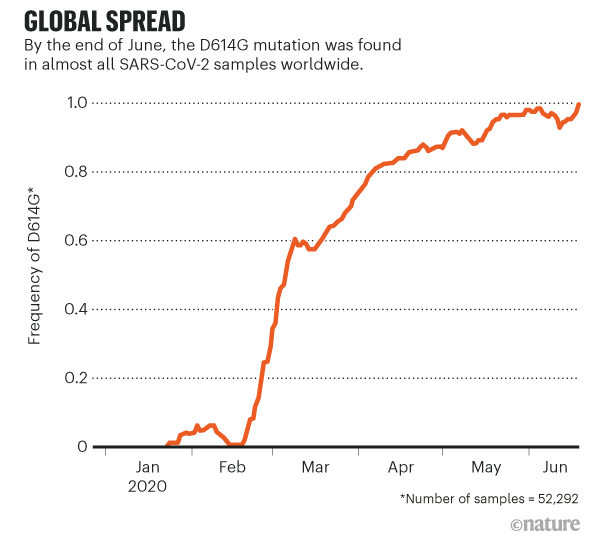
코버는 D614G가 유럽에서 신속하게 증가하고 있다는 데 주목했다. 상당수의 대륙들이 록다운에 들어간 3월 전에만 해도, 야생형 바이러스('D' 바이러스라고 하자)와 변이 바이러스('G' 바이러스라고 하자)가 모두 존재했지만, 대부분의 서유럽 국가에서 D 바이러스가 유행했다. 그런데 3월이 되면서 유럽 전역에서 G 바이러스의 출현빈도가 증가했고, 4월이 되자 지배적인 세력으로 부상했다(참고 1, 참고 2).
그러나 'G 바이러스를 선호한 자연선택'은 이상(以上)과 같은 패턴을 설명하는 '유일한'(또는 심지어 '가장 유력한') 요인이 아니다. G 변이체가 유럽을 지배한 것은 단지 우연으로 치부될 수 있다. 가령 유럽에 처음 도착한 바이러스들 중에서, 어쩌다 보니 G 변이체가 약한 더 흔했다고 치자. 그렇다면 무주공산(바이러스에 취약한 사람들이 널려 있는)인 유럽에서 확산된 바이러스 중 대부분은 소수의 개인에서 비롯된 것처럼 보일 것이다. 따라서 오늘날 G가 유럽을 점령한 것은 순전히 운(운명의 여신이 G를 선택함)이었다. 이것을 창시자효과(founder effect)라고 하는데, 바이러스들 사이에서 흔히 발견되는 현상이다. 특히 바이러스가 (SARS-CoV-2가 3월 중순부터 말까지 유럽의 상당부분에서 그랬던 것처럼) 은밀히 퍼져나갈 때는, 창시자효과가 크게 작용한다.
코버와 동료들은 지난 4월 발표한 출판전 논문에서(참고 1), "캐나다, 호주, 미국의 일부에서 D614G가 신속히 지배세력으로 부상했다"(단 아이슬란드에서는 예외적으로, 집단감염 초기에 존재했던 G 바이러스가 D 바이러스에게 압도당했다)는 사실을 보임으로써 창시자효과를 배제하려고 노력했다. 그들은 영국 셰필드의 병원 입원자 데이터를 분석하여, "G 바이러스에 감염된 사람들의 증상이 악화됐다는 증거는 없다"고 보고했다. 그러나 G 바이러스에 감염된 사람들은 D 바이러스에 감염된 사람들에 비해 코와 구강에서 약간 높은 수준의 바이러스 RNA가 검출되었다.
많은 과학자들은 'D614G의 증가가 괄목할 만하다(또는 팬데믹의 전부를 설명한다)'는 주장을 납득하지 않았다. "나는 그 출판전 논문이 믿을 수 없을 만큼 섣부르다고 생각했다"고 시헌은 말한다.
"D614G에 대한 나와 코버의 관점은 'HIV 연구'에 의해 형성되었다. HIV의 경우, 외견상 무의미한 변이일지라도 면역계의 바이러스 인식능력에 심오한 영향력을 발휘한다"고 몬테피오리는 말한다. "우리는 D614G에 놀라, 그게 백신에 미치는 영향을 알아낼 필요성을 느꼈다."
실험실 연구 러시
(1) 'D614G가 바이러스의 전염력을 증가시켰다'는 가설을 더욱 면밀히 검증하기 위해, 몬테피오리는 실험실 조건에서 그 변이의 효과를 측정했다. 그는 실험실에서 천연 SARS-CoV-2를 연구할 수 없었는데, 그 이유는 생물안전성 밀폐(biosafety containment)가 요구되기 때문이었다. 그래서 그는 (SARS-CoV-2의 스파이크를 이용해 세포를 감염시키는) 유전자변형 HIV를 연구했다. 그런 슈도바이러스(pseudovirus) 입자는 바이러스 연구실의 견인차로서, 치명적 병원체(예: 에볼라 바이러스)의 안전한 연구를 가능케 하며, 변이의 효과 검사를 용이하게 해 준다.
지난 6월 '슈도바이러스를 이용한 D614G 연구' 결과를 처음 보고한 연구팀은, 스크립스 연구소(캘리포니아 라오야 소재)의 바이러스학자 최혜련과 마이클 파잔이었다(참고 3). 뒤이어 많은 연구팀들이 그와 비슷한 연구를 《bioRxiv》에 포스팅했다. [몬테피오리와 동료들의 실험 결과는 《Cell》에 실렸다(참고 2).] 그들은 상이한 슈도바이러스 시스템을 이용하여, 다양한 유형의 세포를 대상으로 테스트했지만 똑같은 결론에 도달했다: "G 바이러스는 D 바이러스보다 훨씬 더 뛰어난 감염능력—어떤 경우에는 최대 10배—을 보유하고 있다."
"실험실 연구에서, 우리 모두는 'D614G가 입자의 감염성을 높인다'는 데 동의했다"라고 매사추세츠 의과대학(우스터 소재)의 제러미 루만(바이러스학)은 말했다. 그러나 그런 연구들에는 많은 한계가 있으며, 인간의 감염에 적용될 수 있을지 불투명하다. "연구자들은 매우 통제된 맥락에서 결론을 도출한 다음, '팬데믹에 큰 시사점을 던진다'고 말하기 일쑤다"고 그루바우는 지적했다. 대부분의 경우, 슈도바이러스는 스파이크 단백질 하나만 달랑 갖고 있으므로, 연구자들은 그것이 세포에 침투할 수 있는 능력만 측정할 뿐, (생명체는 차지하더라도) 세포 내부에서 수행하는 역할은 도외시한다. 또한 슈도바이러스는 (거의 모든 D614G 바이러스들이 보유하는) 3개의 다른 변이를 갖고 있지 않다. "요컨대, 슈도바이러스는 진짜 바이러스가 아니다"라고 루반은 말했다.
(2) 어떤 연구실에서는 현재 '아미노산 한 개만 다른 감염성 SARS-CoV-2'를 갖고서 연구하고 있다. 그들은 실험실에서 인간의 폐 및 기도 세포 배양물을 대상으로 테스트를 하며, 페럿이나 햄스트를 이용한 동물연구도 수행한다. "경험이 풍부하고 생물안전성 능력을 보유한 연구실에게, 그런 연구는 가장 기본적이다"라고 시헌은 말한다. 그런 연구결과를 최초로 발표한 팀은 텍사스 의대(갈베스톤 소재)의 연구팀으로, 9월 2일 출판전 논문을 포스팅했다(참고 3). 그들은 그 논문에서, "G 바이러스는 D 바이러스보다 인간의 폐세포를 더 잘 감염시키며, G 바이러스는 감염된 햄스터의 상기도에 더 많이 존재한다"고 보고했다(참고 4).
하지만 그런 실험조차도 명확한 결론을 내리지 못할 수 있다. 어떤 연구에서는, "MERS 바이러스의 스파이크 단백질에 생긴 '특정 변이'가 생쥐에게 심각한 질병을 초래할 수 있지만, '다른 변이'는 사람이나 낙타(MERS 감염의 저장소)에게 거의 영향을 미치지 않는다"고 보고했다.
'D614G가 사람들 간의 SARS-CoV-2 확산에 미치는 영향'에 대한 명쾌한 해명은 「영국 COVID-19 유전체학 컨소시엄(COVID-19 Genomics UK Consortium)」이라는 야심찬 노력에서 나왔다. 그 컨소시엄은 약 25,000개 바이러스 샘플의 유전체를 분석함으로써 영국에 도입되어 확산된 바이러스의 사례를 1,300건 이상 확인했는데, 그중에는 D 바이러와 G 바이러스도 포함되어 있다.
컨소시엄에 소속된 영국 에든버러 대학교의 앤드루 램보트(진화생물학), 임페리얼칼리지런던(ICL)의 에릭 볼츠(역학), 카디프 대학교의 토머스 코너(생물학)는 62건의 D 바이러스 집단감염과 245건의 G 바이러스 집단감염을 연구했다(참고 5). 그들은 "두 가지 바이러스에 감염된 사람들의 임상적 차이를 발견하지 못했지만, G 바이러스가 D 바이러스보다 약간 더 빨리 전파되는 경향이 있으며, 감염집단의 규모도 더 큰 것으로 나타났다"고 보고했다. 그들이 추정한 전파속도의 차이는 약 20%이지만, 진정한 차이는 더 클 수도 있고 더 낮을 수도 있다. 그러나 램보트에 의하면, 절대적인 차이는 크지 않다고 한다.
"D614G는 일종의 적응으로서, '사람의 세포에 침투하거나 야생형 바이러스와의 경쟁에서 승리하는 것을 도와주지만, 사람들 간(또는 집단 내)의 확산 속도에는 별로 영향을 미치지 않는다'는 특징을 가졌을 수 있다"고 램보트는 말했다. "그것은 사람이나 일부 인간세포에 제대로 적응했지만, 그 이상의 변화를 의미하지 않는다. 사람에게 적응했다고 해서, 확산속도가 빨라지라는 법은 없다"고 그루바우는 거들었다.
(3) 그루바우의 견해에 따르면, D614G는 지금껏 과학자들로부터 지나친 관심을 받았는데, 그 이유는 세간의 이목을 끄는 논문이 발표되었기 때문이다. "과학자들은 영문도 모른 채 D614G라는 변이의 광팬이 되었다"고 그는 말했다. 그러나 그는 D614G를 다른 관점에서 바라보고 있는데, 그 내용인즉 '유전적 다양성의 측정에서 볼 때 이렇다 할 만한 것이 없는 바이러스'를 배우는 방법이 될 수 있다는 것이다. "바이러스 학자의 관점에서 볼 때, D614G는 많은 학문적 흥미로움을 자아낸다"고 그루바우는 말했다.
루반도 그루바우의 견해에 공감한다. "D614G를 집중적으로 연구하면, SARS-CoV-2가 세포와 융합하는 메커니즘을 설명하는 데 많은 도움이 될 것이다"라고 루반은 말했다. '바이러스와 인간세포의 융합'은 약물로 차단하거나 백신으로 정조준해야 할 과정이다. 7월 16일 《bioRxiv》에 포스팅한 슈도바이러스(참고 6)의 업데이트 버전으로, 루반이 이끄는 연구팀은 저온전자현미경(cryo-electron microscopy)을 이용하여 D614G를 포함하는 스파이크 단백질의 구조를 분석했다. 스파이크 단백질은 3개의 동일한 펩타이드로 구성되어 있는데, 각각의 펩타이드는 '개방형'과 '폐쇄형'이라는 방향성을 갖고 있다. 선행연구에서는 "바이러스 입자가 숙주의 세포막과 융합하려면, 3개의 펩타이드 중 최소한 2개가 개방되어야 한다"고 제안했고(참고 7), 루반이 이끄는 연구팀은 "G 바이러스의 스파이크가 개방될 가능성이 훨씬 더 높다"는 사실을 발견했다. 코버의 LANL 동료인 한드라세가람 그나나카란의 지휘 하에 몬데피오리와 코버가 수행한 컴퓨터 모델링 연구에서도 그와 똑같은 결론이 나왔다(참고 8). "G 변이체의 스파이크는 D 바이러스의 스파이크와 다른 방식으로 작동하도록 설정된 것 같다"고 루반은 말했다.

G 바이러스는 항체를 회피할 수 없다, 아직은
대부분의 입수 가능한 증거에 따르면, D614G는 몬테피오리가 우려했던 것과 달리 '면역계의 중화항체가 SARS-CoV-2를 인식하는 것'을 막을 수 없는 것으로 보인다. 왜냐하면 그 변이가 스파이크 단백질의 수용체결합영역(RBD: receptor-binding domain)에 존재하지 않기 때문이다. RBD는 많은 중화항체들이 겨냥하는 표적으로, (바이러스가 세포 안으로 침입하는 데 있어서 핵심단계인) 세포 수용체 단백질 ACE2에 결합한다.
그러나 '다른 변이들이 바이러스로 하여금 일부 항체를 회피하게 할 수 있다'는 증거가 보고되고 있다. 록펠러 대학교 뉴욕시 캠퍼스의 테오도라 하지이오아누와 폴 비니아즈가 이끄는 연구팀은 (SARS-CoV-2의 스파이크 단백질을 사용해 세포를 감염시킬 수 있도록) 가축의 병원체인 수포성구내염바이러스(vesicular stomatitis virus)의 유전체를 변형하여, 중화항체의 존재 하에서 배양했다. 그들의 의도는, 스파이크 단백질로 하여금 항체의 인식을 회피하도록 해 주는 변이를 선택하는 거였다. 그리하여 탄생한 스파이크 단백질 변이체는 'COVID-19에서 회복한 환자의 혈액에서 채취한 항체'는 물론 '치료용으로 개발된 강력한 단클론항체'에도 저항성을 보였다. "우리가 만든 스파이크 단백질 변이체 중에서, 환자에게서 분리된 바이러스의 시퀀스에서 발견되지 않은 것은 하나도 없다. 단, 빈도가 매우 낮은 것으로 보아, 그 변이가 양성선택(positive selection)을 통해 일반화되지는 않은 듯하다"고 그들은 말했다(참고 9).
다른 과학자들은 '어떤 변이가 중요할 것인지'를 예측함으로써 SARS-CoV-2의 진화를 앞지르려 하고 있다. 워싱턴주 시애틀 소재 프레드 허친슨 암 연구센터(Fred Hutchinson Cancer Research Center)의 면역학자 제시 블룸이 이끄는 연구팀은 약 4,000개의 'RBD 변이 버전'을 창조하여, 그 변이들이 '스파이크 단백질의 발현'과 '스파이크 단백질의 ACE2 결합능력'에 미치는 영향을 측정했다. 그 결과 대부분의 변이들은 스파이크 단백질의 속성(발현량과 결합능력)에 영향을 미치지 않는 것으로 밝혀졌지만, 극소수가 두 가지 속성을 향상시키는 것으로 나타났다(참고 10). 그런 변이 중 일부는 COVID-19 환자에게서 확인되었지만, 연구팀은 자연선택의 징후를 전혀 발견하지 못했다고 한다. "현재로서, SARS-CoV-2는 ACE2에 결합하는 데 부족함이 없는 듯하다"고 블룸은 말했다.
블룸 팀은 그런 변이들이 바이러스로 하여금 항체의 공격을 무력화시키는지 여부를 테스트하지 않았다. 그러나 그들의 연구결과가 시사하는 것은, 그런 변이가 가능하다는 것이다. "SARS-CoV-2가 '항체에 대한 취약성'과 '면역력'을 바꾼 변이를 획득한다는 것은 가능하지만, 꼭 그러리라는 보장은 없다"고 블룸은 말했다.
다른 코로나바이러스에 대한 경험에 기반하여 유추해 보면, 그런 변이가 생기려면 수년이 걸릴 것으로 보인다. 여러 시즌에 걸쳐 수집된 보통감기 코로나바이러스(common-cold coronavirus)를 연구한 결과에 따르면, 면역력에 대응한 진화(evolution in response to immunity)의 징후가 일부 엿보인다. "그러나 변이의 페이스는 매우 느리다"라고 스위스 베른 소재 바이러스 및 면역학 연구소(IVI: The Institute of Virology and Immunology)의 볼커 틸(RNA 바이러스학)은 말했다. "그런 변이체들은 다소 일정한 상태를 유지한다."
대부분의 지구촌 주민들이 SARS-CoV-2에 감수성을 지니고 있는 한, 면역력이 바이러스 진화의 주요 요인이 될 가능성은 낮다. 그러나 "감염을 통해서든 백신접종을 통해서든 집단면역 수준이 증가하면, '면력을 회피하는 변이'의 방울(trickle)이 지속적으로 축적되어 영속성을 획득할 수 있다"고 시헌이 말했다. 시헌의 말대로라면, 이전 감염에 대한 면역력이 일부 잔존하는 사람들은, 변이된 바이러스에 감염될 경우 대체로 경미한 증상을 겪게 될 것이다. "나는 SARS-CoV-2가 '더욱 흔한, 감기를 초래하는 코로나바이러스'로 자리 잡는다 해도 전혀 놀라지 않을 것이다." 그러나 코로나바이러스(SARS-CoV-2 포함)에 대항하는 우리의 면역반응이 매우 강력하거나 장기적으로 지속된다면, 그것이 선택압(selection pressure)으로 작용함으로써 상당히 변형된 바이러스(significantly altered virus strain)를 탄생시킬 가능성도 배제할 수 없다.
만약 단클론항체 요법을 현명하게 사용하지 않는다면—가령 COVID-19 환자가 하나의 항체를 주입받았는데, 그게 하나의 바이러스 변이에 의해 무력화된다면—, 우려스러운 변이가 더욱 흔해질 수 있다. 연구자들에 따르면, 단클론항체의 칵테일(각각의 항체들이 스파이크 단백질의 여러 영역을 인식한다)을 이용해 '특정 변이가 자연선택을 통해 선호될 가능성'을 낮출 수 있다고 한다. 그러나 백신의 경우에는 그런 문제점이 발생할 가능성이 낮다. 왜냐하면 백신은 인체의 면역반응과 마찬가지로, 다양한 항체들을 촉발하는 경향이 있기 때문이다.
심지어, 몬테피오리 팀이 지난 7월 《bioRxiv》에 업로드한 논문에 따르면(참고 11), D614G 변이가 SARS-CoV-2를 '백신의 손쉬운 표적'으로 만들 수도 있다고 한다. 즉, 생쥐, 원숭이, 사람에게 수많은 실험용 RNA 백신(이를테면 화이자가 개발한 RNA 백신) 중 하나를 접종했더니, D 바이러스보다 G 바이러스에 더욱 강력하게 반응하는 항체를 생성했다는 것이다.
"G 바이러스가 보편화된 현실을 감안할 때, 그것은 희소식이 아닐 수 없다"고 몬테피오리는 말했다. 그러나 HIV가 수많은 백신을 요리조리 피하는 것을 봐 온 과학자로서, 그는 SARS-CoV-2가 인간의 면역반응을 회피할 수 있는 잠재력을 우려하고 있다. 루반도 몬테피오리의 견해에 동의한다: "우리는 추가적인 변이에서 한 순간도 눈을 떼지 말아야 한다."
※ 참고문헌
1. https://doi.org/10.1101/2020.04.29.069054
2. https://doi.org/10.1016%2Fj.cell.2020.06.043
3. https://doi.org/10.1101/2020.06.12.148726
4. https://doi.org/10.1101/2020.09.01.278689
5. https://doi.org/10.1101/2020.07.31.20166082
6. https://doi.org/10.1101/2020.07.04.187757
7. https://doi.org/10.1126%2Fscience.abb2507
8. https://doi.org/10.1101/2020.07.26.219741
9. https://doi.org/10.1101/2020.07.21.214759
10. https://doi.org/10.1016%2Fj.cell.2020.08.012
11. https://doi.org/10.1101/2020.07.22.20159905
